天然产物一直是药物研发的重要资源,但通过传统的分离方法发现的新型天然产物越来越少。而随着近些年基因测序和生物信息学分析技术的发展,大量未鉴定的基因簇被发现,表明了微生物产生天然产物的巨大潜能,因此,如何挖掘和激活这部分潜能是新天然产物发现的关键。
近日,57365最快最新检测中心、医药生物技术国家重点实验室的戈惠明和谭仁祥教授研究团队在使用基因组数据挖掘发现活性天然产物及其生物合成研究中取得重要进展,相关成果“Comparative Genome Mining and Heterologous Expression of an Orphan NRPS Gene Cluster Directs the Production of Ashimides“2019年1月在线发表于英国皇家化学会旗舰刊物Chemical Science ,论文链接为http://dx.doi.org/10.1039/C8SC05670F 。博士生史净为该论文第一作者,谭仁祥和戈惠明教授是该论文的共同通讯作者。
非核糖体肽类化合物( Nonribosomal peptides,NRPs)是重要的临床药物分子的来源,比如免疫抑制剂环孢菌素A、抗生素万古霉素等,它们是由模块化的非核糖体肽合成酶( nonribosomal peptide synthetase,NRPS )生产线组装多个氨基酸形成。每个非核糖体肽合成酶组装的氨基酸与该酶的结构有关。基于此特性,研究组通过基因组挖掘技术在海洋放线菌Streptomyces sp. NA03103 中找到了一个非核糖体肽类合成的孤儿基因簇(asm),该基因簇比较特殊,一是在已知基因数据库中并没有发现同源基因簇;二是每个核糖体肽合成酶都是单模块的,而非常见的多模块。为获得该基因簇编码的天然产物,研究人员通过构建cosimid文库完整抓取了该基因簇,并在异源宿主中成功表达得到了相应的产物 ashimide A 与ashimide B,其中含氯化合物ashimide B 对肿瘤细胞有中等的细胞毒活性。
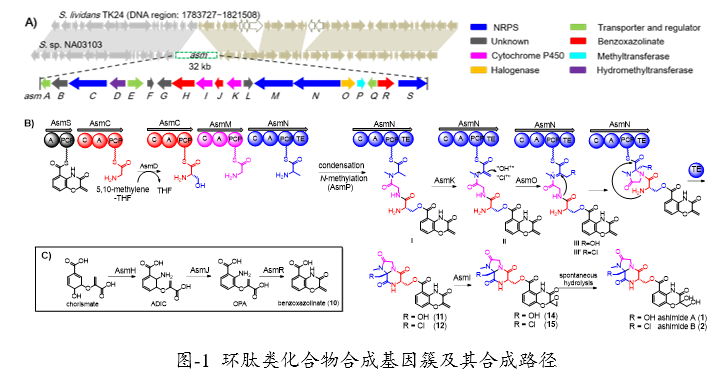
通过对异源表达菌株的基因敲除、同位素标记、体外酶反应等实验,研究组进一步阐释了ashimide 的生物合成过程:基因簇中的4 个单模块NRPS 分别识别benzoxazolinate、甘氨酸、甘氨酸、丙氨酸,在丝氨酸羟甲基转移酶 AsmD 将 AsmC 识别的甘氨酸转变为丝氨酸后,四个单模块NRPS 依次组装各自所识别底物形成不成熟的产物;在甲基转移酶AsmP、P450单加氧酶AsmK 等后修饰酶作用下,形成产物中间体,该中间体被卤化酶AsmO识别后,发生卤化反应,随后引起分子内的反应形成含有imidazolidin-4-one 环的前体产物;最后前体产物在TE 模块的催化下环化后从NRPS 上解离下来,被AsmI 环氧化修饰后,自发水解形成ashimide A 与ashimide B 。该项研究阐明了一个通过氧化、卤化以及环化一系列反应产生复杂结构的过程。此研究过程通过使用的基因组发掘、异源表达等技术达成,进一步说明了此类技术在新型天然产物应用的巨大前景。
该工作得到生科院孙洋和徐强教授课题组的支持,并且得到了国家自然科学基金委优青项目、重点项目、科技部以及中央高校基本科研业务费等的资助,在此表示感谢。