近期,国际著名期刊【Chemical Science】以封面文章发表了我校57365最快最新检测中心李根喜教授课题组在生物分子工程及临床检验应用方面的一项成果,并且被作为热点论文加以介绍。酶联免疫分析是生物医学研究及临床检验中最常用的技术手段,但存在检测信号单一、检测灵敏度较低等问题。李根喜教授课题组首次实现了酶联免疫分析的同时多色检测,极大地弥补了传统酶联免疫测定中效率低下的问题,并且证实了联合分析病人血清中三种肿瘤标志物,可以显著提高肺癌的检出率,为癌症的早期诊断和对症施治提供了非常有益的信息。在这一工作中,他们通过将抗体分子修饰在富含羧基的石墨烯边缘,然后再通过π-π相互作用和疏水作用力将多种变色分子如孔雀石绿、甲基红、酚酞、百里酚酞分别吸附到石墨烯表面,从而制得多种pH响应的变色纳米探针,因此实现了多种肿瘤标志蛋白的多色分析。相关成果以“Improvement of enzyme-linked immunosorbent assay for the multicolor detection of biomarkers”为题发表于【Chemical Science, 2016, 7, 3011-3016】。
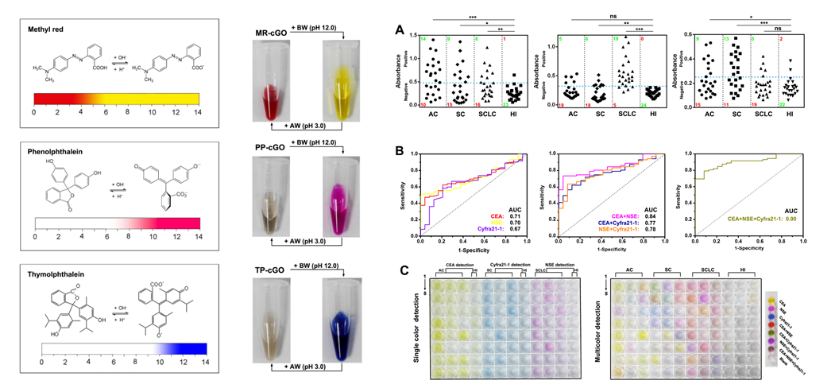
图1:pH响应的纳米探针用于肿瘤标志蛋白的多色分析。
李根喜教授课题组长期从事生物分子工程及临床检测应用方面的研究工作,近期与南京医科大学附属第一医院(江苏省人民医院)、附属第二医院、以及南京大学附属鼓楼医院的有关专家合作,在疾病标志蛋白分析新方法及临床检验应用方面取得了系列进展,为临床医学诊断和治疗提供了全新的技术路径。例如,疾病蛋白标志物的发现为相关疾病(如肿瘤、心血管疾病等)的快速、准确诊断带来了新的契机,然而在疾病发生的早期阶段,这些标志物的浓度很低,现有的检测方法往往对此无能为力,为此,李根喜教授课题组利用“DNA步行者”的基本原理,设计了一种全新的电化学生物传感器,可以用于多种临床上常用疾病标志物的灵敏检测。在这一工作中,他们通过设计一种双功能DNA探针,其一端的功能区域可以特异性地识别待测物,另一端的功能区域则能够与电极界面上事先修饰好的信号DNA短链互补配对形成DNA核酶。当待测物存在时,多个双功能DNA探针可以与待测物形成类似于“DNA步行者”的组装体,在邻位效应的帮助下,组装体通过多个双功能DNA探针与电极上信号链的结合,形成完整的核酶切断信号链,而热稳定性的变化促使双功能DNA探针脱离下来,继续结合下一个信号链并将其切割,从而形成有效的放大效应。研究结果证明该检测体系可实现大范围(10-18-10-9 M)和高灵敏度(10-18 M)疾病标志物的检测,为疾病的早期诊断提供了有利的工具,同时,该研究也为利用DNA机器来构建蛋白质电化学检测方法提供了新的设计思路。相关成果以Simple electrochemical sensing of attomolar protein using fabricated complexes with enhanced surface binding avidity为题发表于【Chemical Science, 2015, 6, 4311-4317】。
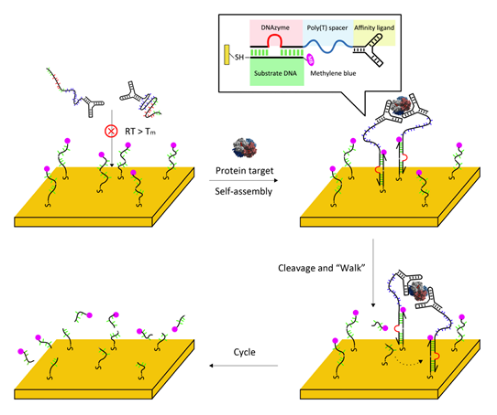
图2:基于DNA“步行者”的电化学传感器用于蛋白质分析示意图。
再如,肿瘤分型与分期的鉴定对确定治疗方案和判断病人的预后有着非常重要的意义,目前临床上常用的分析方法是组织学病理检测,但是基于少量瘤组织切片进行分级,常常难以准确反映整个肿瘤的分化程度,而且容易受到分析人员主观因素的干扰,使分级的价值受到影响,因此,他们提出了一种由石墨烯与DNA修饰的金纳米颗粒组成的比色传感器阵列,可以快速、准确的鉴定出非小细胞肺癌两种最常见的亚型――肺腺癌与肺鳞癌及其三种分期,而且检测过程简单,无需仪器即可完成肉眼可分辨的检测,方便实际应用,相关成果以An array-based approach to determine different subtype and differentiation of non-small cell lung cancer为题发表于【Theranostics, 2015, 5, 62-70】。
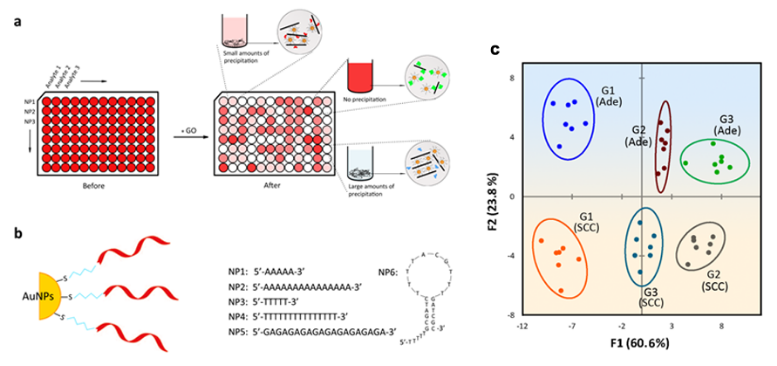
图3:基于ssDNA-GNPs-GO体系的比色阵列用于肺癌分型与分期的鉴别。
近日,【Scientific report】以Enzymatically Regulated Peptide Pairing and Catalysis for the Bioanalysis of Extracellular Prometastatic Activities of Functionally Linked Enzymes为题发表了李根喜教授课题组的另外一项成果(www.nature.com/articles/srep25362) :他们利用新型生物传感分子探针,针对肿瘤的侵袭过程,发展了酶活性与生物学功能分析的生物传感新技术。在这一研究工作中,他们通过将各种蛋白酶、转肽酶的活性变化转化为卷曲螺旋多肽双链的互补配对、解离等明显的构象变化,并进而用这种构象变化控制多肽与金属离子的配位作用,最终将酶活性变化转化为过渡金属离子催化的化学级联放大反应,从而可产生灵敏的生物传感信号。利用该方法,他们在乳腺癌的临床样本中可以观测到血浆素、组织转肽酶及酪氨酸羟化酶等的活性与肿瘤病情发展阶段所呈现出的平行性。该检测方法灵敏度高,且能够分析多种介导肿瘤侵袭、癌基质变性的关键蛋白质的活性,未来肿瘤诊断和预后提供了更加可靠的技术保证。
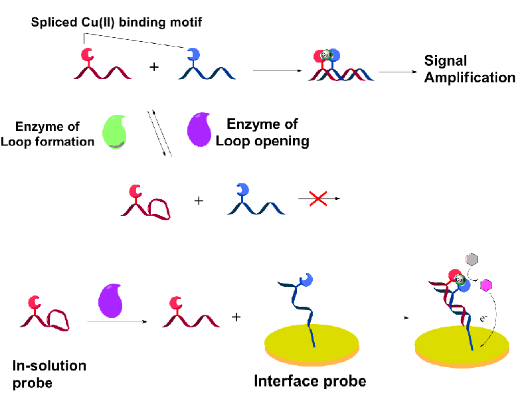
图4 基于多肽构象探针构建的肿瘤侵袭标志蛋白活性检测
以上研究得到国家自然科学基金重点项目、以及教育部创新研究团队的经费支持。