癫痫是最常见的神经系统疾病之一,发病率接近1%,其中约30%的患者会发展为药物难治性癫痫,尤其是伴有海马硬化的颞叶性癫痫患者,此部分患者除手术外,治疗方法十分有限。颞叶性癫痫患者致痫区的两大主要病理学特征是神经元死亡和胶质瘢痕的产生,胶质瘢痕的主要组成细胞是反应性星形胶质细胞。然而,在癫痫病理进程中,反应性星形胶质细胞的功能及其分子机制仍不清楚。
近日,我院闫超教授、陈迪俊教授联合南京大学医学院附属鼓楼医院神经外科刘翔宇主任,首次揭示了颞叶性癫痫患者的大脑中存在一种新的反应性星形胶质细胞亚群——脂质堆积的反应性星形胶质细胞(lipid-accumulated reactive astrocyte, 简称LARA);LARA以依赖APOE的方式形成,表现出独特的分子表型和功能表型;LARA通过上调腺苷A2A受体表达,降低谷氨酸的重摄取,进而加剧神经元的兴奋性,促进癫痫的疾病进展。该发现可以为治疗耐药性癫痫提供全新的策略。

研究人员首先通过分析颞叶性癫痫(temporal lobe epilepsy, TLE)患者的磁共振成像波谱数据,发现患者的致痫侧海马中存在脂质异常堆积,进一步的免疫荧光和脂代谢组学实验表明脂质堆积是TLE患者的重要病理特征,并且脂质堆积主要发生在神经元和星形胶质细胞中。进一步通过收集TLE患者脑组织样本进行单核RNA测序发现,TLE患者中星形胶质细胞脂代谢和脂转运信号通路异常激活,并且载脂蛋白APOE在星形胶质细胞中显著上调。接下来研究者在癫痫小鼠模型中发现,星形胶质细胞特异性APOE敲除能有效改善星形胶质细胞中的异常脂堆积;体外细胞实验结果也表明神经元过度兴奋产生的大量脂质会被星形胶质细胞来源的APOE转运到星形胶质细胞,导致其异常脂堆积。研究人员发现,这些脂堆积异常的星形胶质细胞是一群新的反应性星形胶质细胞。根据单核RNA测序数据,他们鉴定出一个高表达APOE的星形胶质细胞亚群,并表征了其转录组特征,研究者将这个亚群定义为“脂堆积的反应性星形胶质细胞”,英文简称为LARA。
为了探究LARA在癫痫病理中的作用,研究人员对APOE敲除小鼠中进行癫痫造模,发现APOE敲除能有效改善癫痫症状,也能逆转绝大部分LARA相关基因的表达水平,表明APOE是LARA形成的必要条件,且LARA具有促癫痫的作用。最后,研究团队还初步探索了LARA促癫痫的潜在分子机制,发现LARA通过上调腺苷A2A受体来发挥促癫痫作用。使用腺苷A2AR抑制剂或特异性敲低星形胶质细胞的腺苷A2A受体,都能够改善模型小鼠的癫痫症状。
综上,这项研究发现TLE患者病灶区存在异常脂堆积现象,定义了一种全新的反应性星形胶质细胞亚型——LARA,并系统研究了LARA在TLE中的分子表型和功能表型,同时首次揭示了APOE在癫痫疾病进展中的作用,为治疗耐药性癫痫提供了全新的策略。
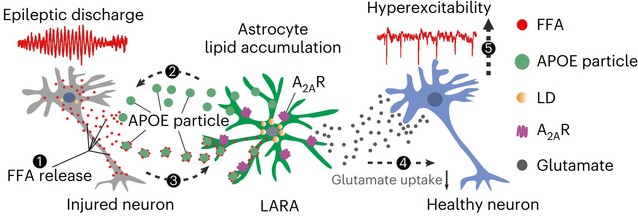
图1. LARA的形成及其促进癫痫进展的原理示意图
该研究成果以“Lipid-accumulated reactive astrocytes promote disease progression in epilepsy”为题,于2023年03月20日发表于神经科学领域顶级期刊Nature Neuroscience。我院闫超教授、医学院附属鼓楼医院神经外科刘翔宇主任、我院陈迪俊教授为该论文的通讯作者;我院助理研究员陈张朋为第一作者兼通讯作者;我院博士生王素吉、赵贤森、方雯为共同第一作者。该工作得到国家自然科学基金等项目支持。
原文链接:https://www.nature.com/articles/s41593-023-01288-6